Химическое строение и свойства витамина B1
Содержание статьи
Витамин В1, был первым витамином, выделенным в кристаллическом виде К. Функом в 1912 г. Позже был осуществлен его химический синтез. Свое название — тиамин — получил из-за наличия в составе его молекулы атома серы и аминогруппы.
Тиамин состоит из 2-х гетероциклических колец — аминопиримидинового и тиазолового. Последнее содержит каталитически активную функциональную группу — карбанион (относительно кислый углерод между серой и азотом).
Тиамин хорошо сохраняется в кислой среде и выдерживает нагревание до высокой температуры. В щелочной среде, например при выпечке теста с добавлением соды или карбоната аммония, он быстро разрушается.
В желудочно-кишечном тракте различные формы витамина гидролизуются с образованием свободного тиамина. Большая часть тиамина всасывается в тонком кишечнике с помощью специфического механизма активного транспорта, остальное его количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется тиаминпирофосфокиназой, а затем переносится в другие органы и ткани.
Существует мнение, что основной транспортной формой тиамина является ТМФ.
Витамин В1, присутствует в различных органах и тканях как в форме свободного тиамина, так и его фосфорных зфиров: тиаминмонофосфата(ТМФ), тиаминдифосфата (ТДФ, синонимы: тиамин пирофосфат, ТПФ, кокарбоксилаза) и тиаминтрифосфата (ТТФ).
ТТФ — синтезируется в митохондриях с помощью фермента ТПФ-АТФ-фосотрансферазы:
Основной коферментной формой (60—80 % от общего внутриклеточного) является ТПФ. ТТФ играет важную роль в метаболизме нервной ткани. При нарушении его образования развивается некротизирующая энцефалопатия. После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
Витамин В, в форме ТПФ является составной частью ферментов, катализирующих реакции прямого и окислительного декарбоксилирования кетокислот.
Участие ТПФ в реакциях декарбоксилирования кетокислот объясняется необходимостью усиления отрицательного заряда углеродного атома карбонила кетокислоты в переходном, нестабильном, состоянии:
Переходное состояние стабилизируется ТПФ путем делокализаиии отрицательного заряда карбо-аниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
Аминокислотные остатки белков обладают слабой способностью осуществлять то, что с легкостью делает ТПФ, поэтому апобелки нуждаются в коферменте. ТПФ жестко связан с апоферментом мульти-ферментных комплексов дегидрогеназ а-оксикетокислот (см. ниже).
- Участие ТПФ в реакции прямого декарбоксилирования пировиноградной кислоты (ПВК).
При декарбоксилировании ПВК с помощью пируватдекарбоксилазы образуется ацетальдегид, который под воздействием алкогольдегидрогеназы превращается в этанол. ТПФ является незаменимым кофактором пируватдекарбоксилазы. Этим ферментом богаты дрожжи.
2. Участие ТПФ в реакциях окислительного декарбоксилирования.
Окислительное декарбоксилирование ПВК катализирует пируватде-гидрогеназа. В состав пируватдегидрогеназного комплекса входит несколько структурно связанных ферментных белков и коферментов (см. с. 100). ТПФ катализирует начальную реакцию декарбоксилирования ПВК. Эта реакция идентична катализируемой пируватдекарбоксила-зой. Однако в отличие от последней, пируватдегидрогеназа не превращает промежуточный продукт гидроксиэтил-ТПФ в ацетальдегид. Вместо этого гидроксиэтильная группа переносится к следующему ферменту в мультиферментной структуре пируватдегидрогеназного комплекса.
Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы, включается в главный метаболический путь клетки — цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплек-са активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, ацетоновых тел и других.
Окислительное дскарбоксилирование а-кетоглутатарата катализирует а-кетоглутаратдегидрогеназа. Этот фермент является составной частью цикла Кребса. Строение и механизм действия а-кетоглугарат-дегидрогеназного комплекса схожи с пируватдегидрогеназой, т. е. ТПФ также катализирует начальный этап превращения кетокислоты. Таким образом, от степени обеспеченности клетки ТПФ зависит бесперебойная работа этого цикла.
Помимо окислительных превращений ПВК и а-кетоглутарата, ТПФ принимает участие в окислительном декарбоксилировании кетокислот с разветвленным углеродным скелетом (продукты дезаминирования ва-лина, изолейцина и лейцина). Эти реакции играют важную роль в процессе утилизации аминокислот и, следовательно, белков клеткой.

3. ТПФ — кофермент транскетолазы.
Транскетолаза — фермент пентозофосфатного пути окисления углеводов. Физиологическая роль этого пути заключается в том, что он является основным поставщиком NADFH*H+ и рибозо-5-фосфата. Транскетолаза переносит дву-углеродные фрагменты от ксилулозо-5-фосфата к рибозо-5-фосфату,
что приводит к образованию триозофосфата (3-фосфоглицеринового альдегида) и 7С сахара (седогептулозо-7-фосфата). ТПФ необходим для стабилизации карб-аниона, образующегося при расщеплении связи С2-С3 ксилулозо-5-фосфата.
4. Витамин В1 принимает участие в синтезе ацетилхолина, катализируя в пируватдегидрогеназной реакции образование ацетил-КоА — субстрата ацетилирования холина.
5. Помимо участия в ферментативных реакциях, тиамин может выполнять и некоферментные функции, конкретный механизм которых еще нуждается в уточнении. Полагают, что тиамин участвует в кроветворении, на что указывает наличие врожденных тиаминзависимых анемий, поддающихся лечению высокими дозами этого витамина, а также в стероидогенезе. Последнее обстоятельство позволяет объяснить некоторые эффекты препаратов витамина В, как опосредованных стресс-реакцией.
Переходное состояние стабилизируется ТПФ путем дслокализаиии отрицательного заряда карб-аниона тиазолового кольца, играющего роль своеобразного электронного стока. Вследствие такого протонирования образуется активный ацетальдегид (гидроксиэтил-ТПФ).
Аминокислотные остатки белков обладают слабой способностью осуществлять то, что с легкостью делает ТПФ, поэтому апобелки нуждаются в коферменте. ТПФ жестко связан с апоферментом мульти-ферментных комплексов дегидрогеназ а-оксикетокислот (см. ниже).
Источник
1. Входит в состав тдф: тиамин(атф) ® тдф
-КОФЕРМЕНТ декарбоксилаз альфа -КЕТОКИСЛОТ(ПВК, альфа -КГК)
КОФЕРМЕНТтранскетолазы (фермент пентозногоцикла).
2.Участвует в передаче нервного импульса.
Суточнаяпотребность в витамине B1- 2-Змг. Она возрастает при употреблениив пищу легко усваиваемых углеводов.1000 ккалтребует 0,5мг ТИАМИНА. Источникамивитамина В1 являются дрожжи, гречневаяи овсяная крупа, пшеничная мука грубогопомола, печень, мясо, яйцо, картофель.Приего недостатке в тканях накапливаютсяПВК, альфа -КГК. Страдает в первую очередьнервнаяткань, что проявляется ПОЛИНЕВРИТОМ.Авитаминоз В1 проявляется в видезаболеваниябери-бери:
ПОЛИНЕВРИТЫ(онемение конечностей, парастезии),
Сердечно-сосудистаянедостаточность,
Нарушениеводного обмена (отёки),
Нарушениефункции ЖКТ (нарушение секреции иперистальтики). Особеннонарушается усвоение витамина В1 ухронических алкоголиков.

Устойчивв кислой среде, но разрушается внейтральной и щелочной среде.
Метаболическиефункции витамина В2.
1. Участвует в окислительно-восстановительных реакциях, т.К. Входит в состав фермента фмн
иФАД.
Компонентдыхательной цепи, входит в состав НАДН- ДГ.
Принимаетучастие в окислении жирных кислот,янтарной кислоты, аминокислот.
Суточнаяпотребность в витамине В2 — 2-4мг.
Источникамивитамина В2 являются дрожжи, печень,мясо, хлеб, соя, яйцо.
Гиповитаминози авитаминоз проявляется поражениемэпителия слизистых, роговицы глаз,кожи;
сухостьгуб, поражение слизистой полости рта,трещины на губах, кератиты, васкуляризация
глаз.

Участвуетв образовании НАД и НАДФ.
Компонентдыхательной цепи.
КОФЕРМЕНТразличных дегидрогеназ.
Суточнаяпотребность в витамине РР 20 — 25мг.
Источникамивитамина РР являются дрожжи, говяжьяпечень, рыба, грибы, мука пшеничная,соя, бобы,хлеб, картофель, мясо. Может синтезироватьсяв организме при поступлении с пищейбелкови витамина В6. Гиповитаминозпроявляется в виде пеллагры:
Дерматитс повреждением симметричных участковкожи, повреждённых УФО.
Диарея.
Деменция.
Причиныгиповитаминоза: белковое голодание,недостаток витамина В6.
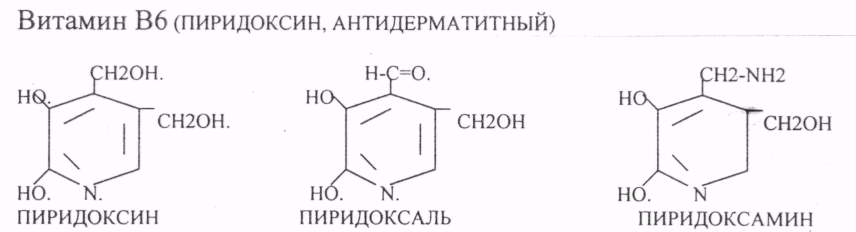
Участвуетв образовании ПФ:
КОФЕРМЕНТАМИНОТРАНСФЕРАЗ.
КОФЕРМЕНТДЕКАРБОКСИЛАЗ.
Принимаетучастие в ДЕЗАМИНИРОВАНИИ.
Необходимдля образования витамина РР из триптофана.
Сигма-АМИНОЛЕВУЛИНОВАЯкислота ®гем.
Т.о.витамин В6 участвует в обмене аминокислот,следовательно, необходим для нормального
обменабелков. Суточнаяпотребность-2мг. Источникивит.В6: картофель, пшеница, рис, отруби,печень, дрожжи. Гиповитаминозприводит к нарушению белкового обмена,что проявляется развитием анемии,дерматита,стоматита, глоссита.
Лекция№ 28. Витамины(продолжение).
ВИТАМИНВ12, ВИТАМИН Н и ПАНТОТЕИНОВАЯ КИСЛОТА.
ВИТАМИНОПОДОБНЫЕСОЕДИНЕНИЯ И АНТИВИТАМИНЫ.
СОСТОЯНИЕВИТАМИННОЙ ОБЕСПЕЧЕННОСТИ В СОВРЕМЕННЫХУСЛОВИЯХ.
ВитаминВ12 (кобаломин,антианемический).
Поструктуре геминоподобное соединение.Устойчив при нагревании, но не образуетсяни в организмечеловека, ни в организме животных, нив растениях, но синтезируетсямикроорганизмами.
Метаболическиефункции витамина В12.
Впроцессе метаболизма из КОБАЛОМИНАобразуются МЕТИЛКОБАЛОМИН иАДЕНОЗИНКОБАЛОМИН.МЕТИЛКОБАЛОМИН участвует в транспортеметильных групп
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Источник
Строение коферментов
Коферменты в каталитических реакциях осуществляют транспорт различных групп атомов, электронов или протонов. Коферменты связываются с ферментами:
— ковалентными связями;
— ионными связями;
— гидрофобными взаимодействиями и т.д.
Один кофермент может быть коферментом для нескольких ферментов. Многие коферменты являются полифункциональными (например, НАД, ПФ). В зависимости от апофермента зависит специфичность холофермента.
Все коферменты делят на две большие группы: витаминные и невитаминные.
Коферменты витаминной природы– производные витаминов или химические модификации витаминов.
1 группа: тиаминовые – производные витамина В1. Сюда относят:
— тиаминмонофосфат (ТМФ);
— тиаминдифосфат (ТДФ) или тиаминпирофосфат (ТПФ) или кокарбоксилаза;
— тиаминтрифосфат (ТТФ).
ТПФ имеет наибольшее биологическое значение. Входит в состав декарбоксилазы кетокислот: ПВК, a-кетоглутаровая кислота. Этот фермент катализирует отщепление СО2.
Кокарбоксилаза участвует в транскетолазной реакции из пентозофосфатного цикла.
2 группа: флавиновые коферменты, производные витамина В2. Сюда относят:
— флавинмононуклеотид (ФМН);
— флавинадениндинуклеотид (ФАД).
Ребитол и изоалоксазин образуют витамин В2. Витамин В2 и остаток фосфорной к-ты образуют ФМН. ФМН в соединении с АМФ образуют ФАД.
[рис. изоалоксазиновое кольцо соединено с ребитолом, ребитол с фосфорной к-той, а фосфорная к-та – с АМФ]
ФАД и ФМН являются коферментами дегидрогеназ. Эти ферменты катализируют отщепление от субстрата водорода, т.е. участвуют в реакциях окисления–восстановления. Например СДГ – сукцинатдегидрогеназа – катализирует превращение янтарной к-ты в фумаровую. Это ФАД-зависимый фермент. [рис. COOH-CH2-CH2-COOH® (над стрелкой – СДГ, под – ФАД и ФАДН2) COOH-CH=CH-COOH]. Флавиновые ферменты (флавинзависимые ДГ) содержат ФАД, который в них является первоисточником протонов и электронов. В процессе хим. реакций ФАД превращается в ФАДН2. Рабочей частью ФАД является 2 кольцо изоалоксазина; в процессе хим. реакции идет присоединение двух атомов водорода к азотам и перегруппировка двойных связей в кольцах.
3 группа: пантотеновые коферменты, производные витамина В3 – пантотеновой кислоты. Входят в состав кофермента А, НS-КоА. Этот кофермент А является коферментом ацилтрансфераз, вместе с которой переносит различные группировки с одной молекулы на другую.
4 группа: никотинамидные, производные витамина РР — никотинамида:
Представители:
— никотинамидадениндинуклеотид (НАД);
— никотинамидадениндинуклеотидфосфат (НАДФ).
Коферменты НАД и НАДФ являются коферментами дегидрогеназ (НАДФ-зависимых ферментов), например малатДГ, изоцитратДГ, лактатДГ. Участвуют в процессах дегидрирования и в окислительно-восстановительных реакциях. При этом НАД присоединяет два протона и два электрона, и образуется НАДН2.
Рис. рабочей группы НАД и НАДФ: рисунок витамина РР, к которому присоединяется один атом Н и в результате происходит перегруппировка двойных связей. Рисуется новая конфигурация витамина РР + Н+]
5 группа: пиридоксиновые, производные витамина В6. [рис. пиридоксаля. Пиридоксаль+ фосфорная к-та= пиридоксальфосфат]
— пиридоксин;
— пиридоксаль;
— пиридоксамин.
Эти формы взаимопревращаются в процессе реакций. При взаимодействии пиридоксаля с фосфорной кислотой получается пиридоксальфосфат (ПФ).
ПФ является коферментом аминотрансфераз, осуществляет перенос аминогруппы от АК на кетокислоту – реакция переаминирования. Также производные витамина В6 входят как коферменты в состав декарбоксилаз АК.
Коферменты невитаминной природы – вещества, которые образуются в процессе метаболизма.
1) Нуклеотиды – УТФ, УДФ, ТТФ и т.д. УДФ-глюкоза вступает в синтез гликогена. УДФ-гиалуроновая к-та используется для обезвреживания различных веществ в трансверных реакциях (глюкоуронил трансфераза).

2) Производные порфирина (гем): каталаза, пероксидаза, цитохромы и т.д.
3) Пептиды. Глутатион – это трипептид (ГЛУ-ЦИС-ГЛИ), он участвует в о-в реакциях, является коферментом оксидоредуктаз (глутатионпероксидаза, глутатионредуктаза). 2GSH«(над стрелкой 2Н) G-S-S-G. GSH является восстановленной формой глутатиона, а G-S-S-G – окисленной.
4) Ионы металлов, например Zn2+ входит в состав фермента АлДГ (алкогольдегидрогеназы), Cu2+ — амилазы, Mg2+ — АТФ-азы (например, миозиновой АТФ-азы).
Могут участвовать в:
-присоединении субстратного комплекса фермента;
-в катализе;
-стабилизация оптимальной конформации активного центра фермента;
-стабилизация четвертичной структуры.
Источник
Витамин B1
Витамин В1 (второе название тиамин) также называют антиневритным витамином, так как он имеет очень важное значение в работе нервной системы. Также ему принадлежат ведущие роли в поддержке практически всех видов обмена веществ.
Витамин В1 синтезируется в организме некоторых представителей фауны, к примеру, жвачных животных, однако человек должен получать его извне. Вещество быстро расходуется организмом, и его запасы нужно пополнять. Для этого необходимо правильно разнообразно питаться или обеспечить дополнительное применение витамина В1 в составе витаминных комплексов.
Содержание витамина В1 в продуктах (на 100г)
- Кедровые орехи 34 мг
- Горох 0,8 мг
- Арахис 0,7 мг
- Фасоль 0,5 мг
- Овсяные хлопья 0,4 мг
- Печень 0,4 мг
- Хлеб ржаной 0,18 мг
- Капуста 0,1 мг
Что собой представляет витамин В1?

Это водорастворимое соединение, которое может существовать в виде нескольких «разновидностей»: тиамин, тиамин моно-, ди- и трифосфат. Наиболее распространен тиамин дифосфат. В организме разные формы витамина могут переходить друг в друга.
Продукты питания, богатые витамином В1
Самые высокие дозировки витамина В1 присутствуют в растительной пище. Им богаты цельнозерновой хлеб, бобовые, шпинат, отруби. Меньшие количества содержатся в различных овощах.
В живых организмах витамин В1 находится в составе мышц, печени, почек, за счет чего в мясе и субпродуктах он тоже есть. Интересно, что в свинине тиамина больше, чем в говядине. Также тиамином богат такой продукт как дрожжи. Минимальные его количества присутствуют в молоке и молочных продуктах.
Суточная потребность в витамине В1
В сутки ребенку необходимо от 0,5 до 1,7 мг тиамина. Необходимая дозировка витамина В1 для мужчины составляет 1,6-2,5 мг, для женщины чуть меньше: 1,3-2,2 мг.
Увеличение потребности в витамине В1
Любые состояния, при которых увеличивается расход витамина В1 или затрудняется его поступление в организм, сопровождаются возрастанием потребности в этом веществе.
К повышению потребности приводят:
• Повышенная физическая активность
• Травмы, заболевания
• Частые нагрузки на нервную систему, стрессы
• Период беременности и грудного вскармливания
• Холодное время года
• Сахарный диабет
• Прием «тяжелых» препаратов.
В этих случаях рекомендовано применение витамина В1 в составе специальных высококачественных биологически активных добавок.
Усвоение витамина В1 из пищи
 Вещество достаточно хорошо усваивается из пищи, особенно если питание правильно составленное и разнообразное. К сожалению, есть два фактора, мешающие усвоению витамина и часто встречающиеся в современном мире.
Вещество достаточно хорошо усваивается из пищи, особенно если питание правильно составленное и разнообразное. К сожалению, есть два фактора, мешающие усвоению витамина и часто встречающиеся в современном мире.
Первое — это заболевания желудка, пищеварительных желез (печень, поджелудочная железа) и кишечника. При этом в пищеварительном тракте нарушается усвоение витамина, даже если в пище его достаточное количество.
Второй фактор — это присутствие в рационе большого количества углеводов (макароны мягких сортов, выпечка, сладости). Если Вы хотите, чтобы витамин В1 хорошо усваивался из пищи, соблюдайте умеренность в потреблении углеводов.
Известны и другие продукты, которые при избыточном потреблении угнетают всасывание витамина В1. В этой пище находятся так называемые антитиаминовые факторы. К «противникам» тиамина относят крепкий кофе и чай, а также морепродукты. При умеренном потреблении они полезны, но если присутствуют в рационе постоянно и в больших количествах, это может оказать негативное влияние на всасываемость тиамина.
Биологическая роль витамина В1
В организме тиамин играет множество ролей и является необходимым компонентом различных физиологических процессов. Функции витамина В1 таковы:
• Принимает участие во всех видах обмена веществ, особенно в углеводном. Также при его участии осуществляется метаболизм аминокислот, образование полезных для организма жирных кислот, входящих в состав клеточных мембран. Кроме того, тиамин в значительной степени «отвечает» за превращение углеводов в организме в жиры, с их последующим отложением в жировых депо.
• При участии витамина В1 реализуются функции нервных клеток и передача в них сигналов.
• Вещество необходимо для полноценной работы проводящей системы сердца.
• При его помощи происходит регуляция кислотности желудочного сока.
• Витамин В1 способствует поддержанию устойчивости иммунитета.
• Нужен для обеспечения функции мышц.
• У детей способствует протеканию процессов развития и роста.
Признаки нехватки витамина В1
При значительном недостатке витамина В1 в пище развиваются нарушения в первую очередь со стороны нервной системы. Тяжелые формы гиповитаминоза тиамина приводят к развитию заболеваний бери-бери и синдрома Вернике. Однако и то, и другое встречается редко, особенно в развитых странах.
Чаще недостаток витамина В1 проявляется «легкими» симптомами, такими как слабость, снижение устойчивости к нагрузкам, склонность к депрессиям, сложности в усвоении новой информации, нарушения работы органов пищеварения, развитие невритов и других неврологических заболеваний, бессонница, снижение аппетита.
Признаки избытка витамина В1
Добиться избытка витамина В1 в естественных условиях невозможно, даже если питаться исключительно продуктами с его содержанием. При избыточном поступлении он перестает усваиваться с пищей, так как не может в больших количествах накапливаться в тканях.
Если же «насильно» ввести в организм большую дозу тиамина, возможны опасные последствия. Тиамин при передозировке активизирует механизм аллергии, из-за чего человек может даже погибнуть от симптомов, напоминающих анафилактический шок. К счастью, ни один человек не будет сознательно пытаться отравить себя витамином, так что его избыток маловероятен.
Факторы, влияющие на содержание в продуктах витамина В1

При термической обработке пищи (варка, жарка) витамин В1 разрушается. Именно поэтому, составляя рацион, рекомендуется потреблять больше свежих продуктов с содержанием этого витамина.
К примеру, вместо отварной овсянки можно есть по утрам мюсли из сырых овсяных хлопьев. Пред тем как варить фасоль или горох, их желательно замочить в воде, чтобы они размягчились и сварились быстрее.
Почему возникает дефицит витамина В1
Основными причинами недостатка тиамина являются частые стрессы, нервные переживания, а также неправильное составление питания (употребление избытка углеводов, кофе и т.д.).
Также среди причин гиповитаминоза стоит упомянуть прием алкоголя. У лиц с алкоголизмом иногда отмечаются тяжелые формы недостатка витамина.
Витамин В1: цена и продажа
Если Вы поняли, что Ваш рацион далек от совершенства или что у Вас повышенная потребность в тиамине, для сохранения здоровья Вам рекомендуется принимать витамин В1 дополнительно.
На нашем сайте Вы можете купить витамин В1, приобретя его отдельно или в составе комплексных биодобавок. Цена на препараты витамина В1 различна, у нас представлен широкий выбор средств от разных производителей, принадлежащих к разным ценовым категориям. Среди представленных наименований Вы сможете выбрать самый лучший, доступный вариант, подходящий именно Вам.
Сделать заказ можно двумя способами: добавив выбранный препарат в корзину или созвонившись с нашими менеджерами. Доставка осуществляется по всей стране.
Также на нашем сайте Вы можете получить бесплатную консультацию нутрициолога по приему БАДов и витаминов.
Для регионов действует бесплатный номер 8 800 550-52-96.
Каталог продукции, содержащей витамины группы В
Источник